Berbagi Sastra|Strategi dan contoh pemurnian protein
Ringkasan:
Artikel ini meninjau dua faktor utama yang harus dipertimbangkan dalam strategi pemurnian protein: persyaratan aplikasi hilir dan karakteristik biologis protein itu sendiri. Artikel ini menekankan bahwa pemurnian protein berkualitas tinggi adalah dasar untuk keandalan dan pengulangan data eksperimental, terutama untuk produksi protein rekombinan. Skenario aplikasi yang berbeda memiliki persyaratan spesifik untuk kemurnian protein, aktivitas atau kandungan endotoksin, dan karakteristik protein dapat mempengaruhi strategi pemurnian secara signifikan. Menurut kasus tertentu, artikel tersebut menggambarkan bahwa protein unik harus mengadopsi skema pemurnian yang disesuaikan. Akhirnya, proses produksi protein sistematis diusulkan (Gambar 1), menekankan kontrol kualitas proses penuh dari pemilihan sistem ekspresi, desain konstruksi hingga optimasi pemurnian, dan merekomendasikan evaluasi homogenitas protein dan fungsionalitas melalui teknik biofisik (seperti SEC-MALS, DSF, dll.). Artikel ini bertujuan untuk memberikan panduan praktis bagi para peneliti, membantu mereka merumuskan strategi pemurnian yang efisien dan berulang berdasarkan karakteristik dan persyaratan aplikasi protein target, sehingga meningkatkan kualitas dan efisiensi penelitian ilmiah.

Gambar 1. Diagram skematik proses produksi protein
Produksi Protein Permintaan Tinggi - Contoh identifikasi masalah, desain strategi mitigasi dan output yang sesuai
1. Ikatan asam nukleat dengan protein:
Saat memurnikan protein pengikat asam nukleat, beberapa langkah diperlukan untuk menghilangkan kontaminasi asam nukleat. Selama lisis, nuklease (seperti SM nuclease (Benzonase®) atau DNase atau RNase) perlu ditambahkan, tetapi asam nukleat terikat tidak dapat sepenuhnya dihilangkan. Ganti langkah penghilangan asam nukleat, seperti curah hujan PEI atau streptomisin sulfat, pemurnian heparin atau kromatografi pertukaran ion. Kehadiran asam nukleat dipantau dengan rasio A26 0 nm/a28 0 nm di seluruh proses pemurnian. Jika rasionya lebih rendah dari 0,6, itu menunjukkan bahwa kemurnian protein relatif tinggi dan kontaminasi asam nukleat minimal. Untuk protein dengan asam nukleat yang sangat terikat, mereka dapat sementara terdenaturasi (seperti diobati dengan urea) dan kemudian direnaturasi. Poin-Poin Kunci: Gunakan reagen berkualitas tinggi, buffer segar, dan kolom bersih (bersih dengan 0,5m NaOH sebelum digunakan).
2. Rantai berat ferritin tikus:
Tujuan memproduksi protein rantai berat ferritin mouse (MFTH1) murni adalah mikroskop kri-elektron partikel tunggal resolusi tinggi (Cryo-EM). Vektor ekspresi Escherichia coli yang dikodekan MFTH1 yang tidak berlabel secara ultrasonik terganggu tanpa menambahkan nuclease. Setelah pemanasan pada 7 0 derajat, ia menjalani presipitasi amonium sulfat, dialisis dan ukuran kromatografi eksklusi ukuran. Sampel yang dihasilkan menunjukkan adanya sejumlah besar kontaminan dalam gambar mikroskop cryo-elektron (Gambar 2A), yang sama sekali tidak cocok untuk aplikasinya. Optimalkan langkah -langkahnya. Tambahkan nuclease SM selama proses lisis sel dan proses dialisis setelah presipitasi amonium sulfat, dan kemudian tambahkan langkah kromatografi pertukaran anion untuk mengurangi rasio A26 0 nm/A280Nm dari 1,4 menjadi 0,8. Setelah kromatografi eksklusi ukuran, rasio A260NM/A280NM dari sampel MFTH1 akhir adalah 0,56. Gambar mikroskop SDS-PAGE dan Cryo-Electron (Gambar 2B) menunjukkan bahwa protein sangat murni, menunjukkan bahwa kontaminan telah secara efektif dihapus.

Gambar 2 Rantai Berat Ferritin Mouse
3. Protein chimeric DSRBEC (DSRBD-EGF- chimera):
DSRBEC dibentuk oleh fusi domain pengikat RNA untai ganda (DSRBD) dari protein kinase manusia dan faktor pertumbuhan epidermal manusia (HEGF). Ketika DSRBD diekspresikan dalam Escherichia coli, itu menunjukkan kemampuan pengikatan dsRNA yang sangat tinggi. Setelah lisis sel, RNA kontaminasikan akan menghambat pengikatan protein rekombinan ke kolom afinitas logam afinitas (IMAC). Metode konvensional seperti curah hujan PEI atau streptomisin sulfat, pengobatan RNase atau larutan buffer garam tinggi tidak dapat menghilangkan RNA. Lisis sel dilakukan dengan menggunakan buffer yang mengandung urea 4M. Supernatan dimuat ke kolom iMac, dan 4m ke 0 m urea perlahan digunakan semalam (renaturasi kolom). Buffer renaturasi ditambahkan dengan imidazole dan dielusi dari kolom iMac. Penyempurnaan akhir dilakukan melalui filtrasi gel SuperDex 75 untuk mendapatkan DSRBEC aktif secara fungsional.
4. Protein terikat pada kation divalen atau kofaktor lainnya:
Untuk protein yang berinteraksi dengan kation divalen seperti zn 2+, fe 2+, cu 2+, atau kofaktor lainnya, penting untuk menambahkan kation divalen spesifik (atau kofaktor lain) selama ekspresi. Sejumlah kecil kation divalen yang sama (atau kofaktor lain) juga diperlukan selama proses pemurnian. Namun, penggunaan agen pengkelat (seperti EDTA, EGTA) dan agen pereduksi chelating (seperti DTT atau DTE) harus dihindari. Ketika berhadapan dengan protein yang terikat pada kation divalen, campuran protease inhibitor tanpa agen pengkelat harus digunakan untuk mengkonfirmasi keberadaan aktual kation divalen (atau kofaktor lain) dalam protein yang dimurnikan melalui metode spektroskopi (seperti spektrofotometri penyerapan atom).
5. Ferridoxin Rekombinan (RFD) yang mengandung kluster [2fe ± 2s] tunggal dari cyanobacteria termofilik masterobocladus laminosus
Ferridoxin adalah protein besi-sulfur terlarut yang berpartisipasi dalam reaksi transfer elektron. Ferroredoxin tipe tanaman membawa kluster [2fe ± 2s] tunggal sebagai akseptor elektron fotosistem I. Strain Escherichia coli BL21 (DE3) mengekspresikan protein RFD rekombinan dalam medium TB yang mengandung 10mm FECL3 dan antibiotik. Elusi kolom penangkapan iMac dilakukan dengan menggunakan buffer yang berisi histidin 10mm untuk menghindari imidazol dan mencegah penghancuran cluster [2fe ± 2s]. Pertukaran anion dan kromatografi eksklusi ukuran digunakan untuk pemurnian dan konsentrasi lebih lanjut hingga 12mg/mL untuk skrining kristalisasi. Dibandingkan dengan produksi ferroredoxin rekombinan, ferroredoxin alami yang dimurnikan dari alga biru-hijau Mastigocladus laminosus mencapai resolusi yang lebih tinggi selama kristalisasi.
6. Protein digunakan sebagai antigen
Protein sering digunakan sebagai antigen untuk memulihkan ligan spesifik target. Hal pertama yang perlu dipertimbangkan adalah apakah protein digunakan untuk kekebalan in vivo untuk mendapatkan IgG monoklonal atau poliklonal konvensional, atau untuk program yang melibatkan IgG unta atau proses seleksi in vitro.
6.1 Antigen yang digunakan untuk produksi antibodi rutin
Ketika antigen digunakan untuk menghasilkan antibodi IgG monoklonal, lipatan antigen yang benar biasanya tidak diperlukan, karena sebagian besar antibodi monoklonal mengenali epitop linier yang tidak terlalu dipengaruhi oleh struktur antigen, dan bahkan antigen yang terdenaturasi (seperti protein tubuh inklusi) tetap efektif. Namun, kemurnian harus dikontrol secara ketat untuk menghindari kontaminan imunogenik yang kuat yang mengganggu respons imun dan menyebabkan dominasi antibodi non-target.
6.2 Pemutaran Perpustakaan Konjugasi
Perhatian khusus harus diberikan untuk mempertahankan konformasi alami antigen selama pemrosesan Perpustakaan Nanobody yang diperoleh dengan imunisasi unta. Tidak seperti antibodi konvensional, antibodi unta (terutama nanobodi) cenderung mengenali epitop struktural, yang terkait dengan struktur situs komplementer cembung yang unik. Demikian pula, saat menyaring perpustakaan antibodi sintetis atau alami yang besar secara in vitro, antigen harus mempertahankan struktur yang sepenuhnya konsisten dengan aplikasi target. Karena proses penyaringan itu sendiri tidak bias, jika antigen memiliki kesalahan lipatan, agregasi atau heterogenitas konformasi, sejumlah besar konjugat yang menargetkan epitop non-alami dapat disaring.
7. Protein yang mengandung ikatan disulfida antarmolekul atau intramolekul atau sistein bebas
Ikatan disulfida sangat penting untuk menstabilkan struktur alami protein. Selama proses pemurnian, ketika pemurnian protein yang mengandung ikatan disulfida antarmolekul atau intramolekul, perlu untuk menghindari penambahan agen pereduksi untuk mencegah perubahan konformasi protein, sehingga mengubah fungsinya. Untuk protein yang mengandung sistein bebas, agen pereduksi sangat diperlukan di semua langkah proses pemurnian, terutama selama penyimpanan, untuk mencegah pembentukan ikatan disulfida buatan. Agen pereduksi yang paling umum digunakan adalah dithiothreitol (dtt), -mercaptoethanol (-me), dan Tris (2- carboxyethyl) fosfin hidroklorida (TCEP). Untuk resin iMac yang tidak kompatibel dengan DTT atau TCEP, disarankan untuk menggunakan -Me dan menggantinya dengan agen pereduksi lainnya dalam langkah -langkah berikutnya.
8. Fragmen Antibodi Rekombinan
Meskipun struktur fragmen antibodi rekombinan (seperti nanobodi) lebih sederhana daripada IgG, fungsinya tergantung pada pembentukan ikatan disulfida yang benar. Dalam sistem ekspresi bakteri, bahkan dengan adopsi strategi optimasi, produk yang salah lipatan atau sebagian lipat masih dapat terjadi, yang ada baik di bagian terlarut maupun di badan inklusi. Yang lebih tersembunyi adalah bahwa bahkan fragmen antibodi yang dilipat dengan benar dapat membentuk agregat terlarut (agregasi koloid) melalui plak hidrofobik di permukaan. Agregat semacam itu sulit diidentifikasi dalam tes fungsional rutin (seperti ELISA) karena pengikatan multivalen dapat menutupi penurunan afinitas monomer, tetapi kehadirannya dapat secara serius mempengaruhi aplikasi yang mengandalkan ukuran molekul kecil (seperti mikroskop super-resolusi). Oleh karena itu, hanya mengandalkan SDS-PAGE tidak cukup untuk mengevaluasi kualitas sampel. Metode biofisik seperti filtrasi gel (Gambar 3) harus diadopsi untuk membedakan monomer (puncak utama) dari agregat (puncak volume eksklusi). Titik kontrol utama meliputi: Mengoptimalkan lingkungan redoks selama ekspresi untuk mempromosikan pembentukan ikatan disulfida, dan mengoptimalkan kondisi penyimpanan setelah pemurnian untuk mencegah agregasi. Langkah -langkah ini sangat penting untuk memastikan monodispersitas dan fungsi fragmen antibodi.

Gambar 3. Pemisahan filtrasi gel dari agregat larut nanobodi
9. Fragmen reseptor limfosit LLT1 yang larut
Ekspresi rekombinan protein yang bergantung pada ikatan disulfida (seperti reseptor limfosit LLT1) sering menghadapi kesulitan lipat. Filtrasi gel tipe liar LLT1 menunjukkan puncak agregasi dan puncak dimer (Gambar 4A), tetapi spektrometri massa mengungkapkan kesalahan lipatan yang disebabkan oleh sistein tidak berpasangan dalam dimer (Gambar 4B). Untuk tujuan ini, dua mutan dirancang: satu menghilangkan masalah sistein, menghasilkan penurunan hasil yang tiba -tiba (Gambar 4A); Setelah pengenalan neocysteine untuk merekonstruksi ikatan disulfida yang sesuai, mutan tidak hanya memiliki hasil tinggi dan stabilitas yang baik, tetapi juga dapat mengkristal (Gambar 4C), dan struktur 3D mengkonfirmasi bahwa mutan membentuk ikatan disulfida yang benar dan mempertahankan lipatan alami. Kasus ini menunjukkan bahwa dengan merancang ikatan disulfida konformal secara rasional, dikombinasikan dengan filtrasi gel dan analisis spektrometri massa, masalah lipatan protein rekombinan dapat dipecahkan secara efektif, dan protein fungsional dengan struktur yang stabil dan hasil tinggi dapat diperoleh.

Gambar 4. Rekonstruksi ikatan disulfida meningkatkan lipatan dan hasil LLT1 terlarut
10. Protein yang mudah dikumpulkan
Pemurnian protein rekombinan sering menghadapi masalah agregasi, dan pembentukannya mengikuti mekanisme "pertumbuhan nukleasi"-sejumlah kecil agregat terlarut terbentuk terlebih dahulu dan kemudian memicu agregasi larut skala besar skala besar. Untuk mengatasi tantangan ini, strategi multi-level perlu diadopsi: Pada tahap ekspresi, ini dapat dicapai dengan mengoptimalkan strain, mengurangi suhu kultur, menggunakan media kultur yang dimodifikasi atau berbagai protein fusi pelarutan, dan mengganti sistem ekspresi (sel serangga/mamalia), dll. Selama tahap pemurnian, dalam operasi yang cepat (dalam lingkungan C 4 yang diperlukan untuk menghindari pendirian yang berlebihan). Dtk) harus diadopsi untuk segera menghapus inti agregat. Secara umum, ketika solusi buffer skrining, faktor -faktor seperti komposisi komponen, nilai pH, agen pemisahan atau pelarut harus dipertimbangkan (Gambar 5). Melalui optimalisasi deteksi ortogonal yang baik (seperti SEC, CD, LS, DSF dan pergeseran suhu berdasarkan panas fluoresensi, dll.), Kualitas protein dan larutan buffer yang paling cocok ditentukan.

Gambar 5. Strategi untuk mengurangi agregasi protein
11. Kristalisasi CLK1 Kinase manusia (cara mendapatkan batch yang dapat direproduksi)
Untuk mendapatkan CLK1 kinase non-terfosforilasi yang homogen untuk studi kristalisasi, skema kolaboratif multi-strategi diadopsi. Pertama, itu diekspresikan bersama dengan λ -fosfatase di Escherichia coli untuk menghilangkan heterogenitas autofosforilasi. Meskipun hasilnya berkurang, defosforilasi lengkap dipastikan. Setelah ditangkap oleh iMac, eluen dilengkapi dengan penstabil (arginin 50mm, asam glutamat 50mm dan 10mm DTT) untuk mencegah agregasi, terkonsentrasi, dan labelnya dihilangkan dengan pencernaan TEV. Kemudian, oligomer yang benar dipisahkan oleh SEC (mengandung gliserol 5% dan -Me). Langkah pertukaran anion penting terakhir membedakan antara kelompok CLK1 kristal (non-terfosforilasi) dan non-kristal (sebagian terfosforilasi). Perlu dicatat bahwa mode lisis sel secara signifikan mempengaruhi stabilitas protein-metode tekanan tinggi dan suhu tinggi menyebabkan agregasi CLK1 yang tidak dapat diubah, menyoroti pentingnya pengobatan ringan untuk persiapan kinase.
12. Produk Galectin -1 dengan kemampuan pengikatan ligan yang stabil
Untuk menyiapkan galectin fungsional -1 untuk studi pengikatan ligan, strategi ekspresi dan pemurnian empat konstruksi (galectin tipe liar yang tidak berlabel dan berlabel -1, dibandingkan dengan cysteine mutant galectin {{6}) yang tidak berlabel. Temuan utama menunjukkan bahwa pemurnian kromatografi afinitas laktosa dapat secara efektif menyaring protein yang dilipat dengan benar, tetapi perlu dikombinasikan dengan dialisis menyeluruh (buffer HEPES) untuk sepenuhnya menghilangkan laktosa dari situs pengikatan dan mengembalikan aktivitas CRD. Galectin tipe liar -1 rentan terhadap oksidasi dan inaktivasi, dan stabilitasnya tetap terbatas bahkan di hadapan agen pereduksi (Gambar 6). Namun, mutan bebas sistein secara signifikan meningkatkan stabilitas jangka panjang sambil menjaga aktivitas aglutinasi yang sebanding dan stabilitas termal (diverifikasi oleh nanoDSF, ITC, dll.) Dengan menghilangkan ketergantungan ikatan disulfida.
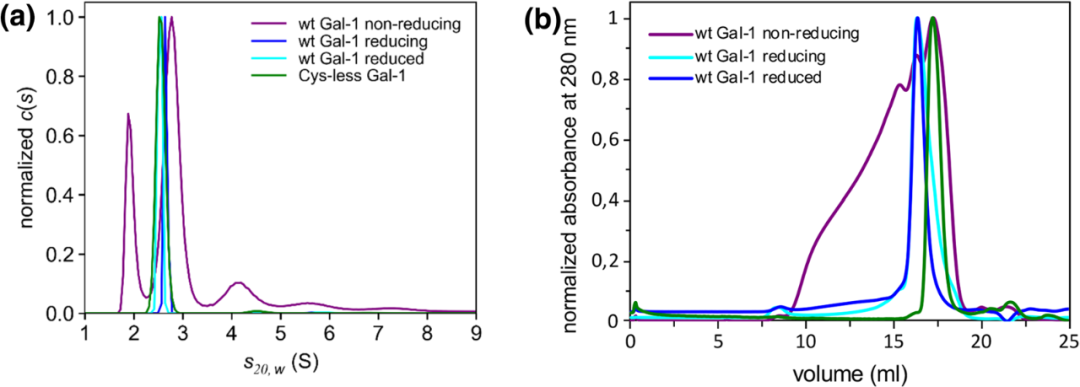
Gambar 6. Karakterisasi hidrodinamik galectin rekombinan -1 mengungkapkan ketidakstabilannya
13. Penghapusan endotoksin
Metode penghapusan endotoksin didasarkan pada kromatografi afinitas termasuk kromatografi bermuatan positif (pertukaran anion), penggunaan ligan polikasionik (seperti poli-l-lisin (PLL), poliamin yang diimobilisasi (polymyxin B)), dan penambahan triton surfaktan X {2}. Selama proses pemurnian, perhatikan menyiapkan larutan buffer dengan air bebas LPS, dan gunakan kolom atau kolom baru yang hanya digunakan dalam pemurnian LPS lainnya. Untuk kontaminasi endotoksin, pompa kromatografi/sistem fluida dapat diinkubasi semalaman di 0. 5m NaOH atau selama 4 jam dalam 1. 0 M NaOH. Jumlah terakhir LPS dalam sampel dievaluasi menggunakan limulus amebocyte lysate reagent (LAL), dan diverifikasi apakah di bawah batas yang diperlukan untuk aplikasi spesifik.
14. Kompleks protein
Ekspresi dan pemurnian kompleks protein perlu dioptimalkan sesuai dengan kondisi tertentu. Tantangan termasuk ketidakstabilan atau kesalahan lipatan subunit. Setiap subunit dapat diekspresikan secara independen dan dirakit secara in vitro, atau diekspresikan bersama untuk membentuk kompleks protein fungsional. Desain konstruksi harus diperkenalkan dengan hati -hati dengan label pemurnian atau deteksi untuk menghindari mengganggu perakitan, terutama ketika informasi yang kompleks terbatas dan beberapa optimisasi diperlukan. Selama proses pemurnian, integritas dan stabilitas kompleks perlu dievaluasi. Metode termasuk SDS-PAGE (deteksi subunit), SEC (homogenitas), SEC-MALS (analisis massa molar), fotometri massa atau spektrometri massa alami (verifikasi massa). Perlu dicatat bahwa kompleks dapat memisahkan pada konsentrasi rendah. Pada saat ini, metode atau buffer kromatografi (seperti melalui drift termal atau kondisi penyaringan DSF) perlu dioptimalkan. Selain itu, mengurangi langkah -langkah pemurnian dapat mencegah hilangnya subunit interaksi yang lemah dan menyeimbangkan efisiensi pemurnian dan integritas kompleks.
15. Pemurnian Kompleks Antigen-Antibodi
Kompleks antibodi-antigen adalah contoh khas kompleks protein. CO-Crystallization mereka dapat mengungkapkan pola pengikatan dan memandu optimalisasi rekayasa antibodi. Metode tradisional membutuhkan pemurnian antigen dan antibodi yang terpisah dan kemudian mencampurnya. Namun, penelitian terbaru menunjukkan bahwa strategi ko-ekspresi dan pemurnian co-for lebih efisien. Hanya satu pemurnian yang diperlukan untuk mendapatkan kompleks, dan pada saat yang sama, antigen yang tidak stabil dapat distabilkan melalui antibodi, dan bahkan ekspresi bebas label dapat dicapai. Dalam situasi khusus ini, SDS-PAGE dan gel filtrasi (SEC) biasanya cukup untuk mengevaluasi kemurnian dan kualitas kompleks.
Ringkasan
Pemurnian protein adalah teknologi mendasar dalam penelitian ilmiah. Produksi protein skala akademik biasanya mengikuti strategi standar dan dapat menghasilkan protein dengan kemurnian tinggi tingkat miligram, yang secara larut, yang banyak digunakan dalam biologi struktural, biokimia dan penelitian fungsional. Namun, persyaratan khusus aplikasi hilir (seperti kebutuhan tidak akan endotoksin dalam percobaan hewan dan tidak ada kontaminasi nuklease dalam penelitian asam nukleat) atau karakteristik yang melekat dari protein (seperti agregasi mudah, yang mengandung ikatan disulfida atau afinitas asam nukleat tinggi) sering memerlukan solusi yang disesuaikan. Tinjauan ini, sebagai tanggapan terhadap keadaan khusus ini, mengusulkan strategi yang disempurnakan mulai dari pemilihan sistem ekspresi, desain konstruksi (mengoptimalkan label dan batas domain) hingga proses pemurnian, dan memperkenalkan kontrol kualitas (seperti SEC, Halaman SDS, deteksi aktivitas, dll.) Pada langkah-langkah utama. Beberapa aplikasi juga memerlukan analisis tambahan (seperti deteksi endotoksin dan penentuan residu asam nukleat), mirip dengan konsep "jaminan kualitas" (QA) dalam industri biofarmasi, yaitu, untuk mencegah cacat melalui proses sistematis. Dengan merumuskan pedoman kontrol kualitas dan mengklarifikasi standar spesifik untuk reagen protein yang digunakan dalam penelitian ilmiah, tujuannya adalah untuk membangun norma pemurnian protein yang lebih ketat untuk laboratorium akademik, meningkatkan keandalan dan pengulangan data eksperimental, dan menjembatani kesenjangan antara penelitian dasar dan standar industri.
Doi: 10.1186/s 12934-022-01778-5

